Actualités

Incendie aux Pennes-Mirabeau / Marseille : soyez vigilants et adoptez les bons gestes !
Un feu de grande ampleur est actuellement en cours aux Pennes-Mirabeau, et a atteint le 16ème arrondissement de Marseille. Nous vous invitons à la plus grande vigilance, et à adopter les bons gestes.

Retour en images sur le vernissage de l’exposition “Femmes Engagées de l’IPC” – Édition #3
Mardi 17 juin, l’IPC a mis à l’honneur des femmes inspirantes lors du vernissage de la 3ᵉ édition de l’exposition « Femmes Engagées de l’IPC », en présence de Madame Caroline Chassin, Directrice générale adjointe, de la photographe plasticienne Julie Lagier, et des collaboratrices sélectionnées par tirage au sort.

Juin Vert, mois de sensibilisation au cancer du col de l’utérus
Juin Vert est un évènement dédié à la sensibilisation autour du cancer du col de l’utérus. Ce dernier peut être évité grâce à la vaccination et au dépistage.

L’Institut Paoli-Calmettes parmi les meilleurs hôpitaux de France selon Le Point – Édition Hors-série 2025
Le hors-série 2025 du magazine Le Point consacre, une fois encore, l’excellence médicale française à travers un palmarès rigoureux et inédit des hôpitaux et cliniques du territoire. L’Institut Paoli-Calmettes y confirme sa place de centre de référence en cancérologie, avec plusieurs spécialités classées parmi les meilleures au niveau national.

10 ans IPC3 : Une décade de soin, d’innovation et d’espoir pour le bâtiment IPC3 !
En cette année 2025, nous célébrons le centenaire de l’Institut Paoli-Calmettes ; mais nous souhaitons également mettre à l’honneur le bâtiment IPC3, qui fête sa première décennie !

Congrès de l’ASCO : les experts IPC présents à Chicago !
Vendredi 30 mai a débuté le congrès annuel de l’American Society of Clinical Oncology (ASCO). Il se tient à Chicago jusqu’à demain, mardi 3 juin.
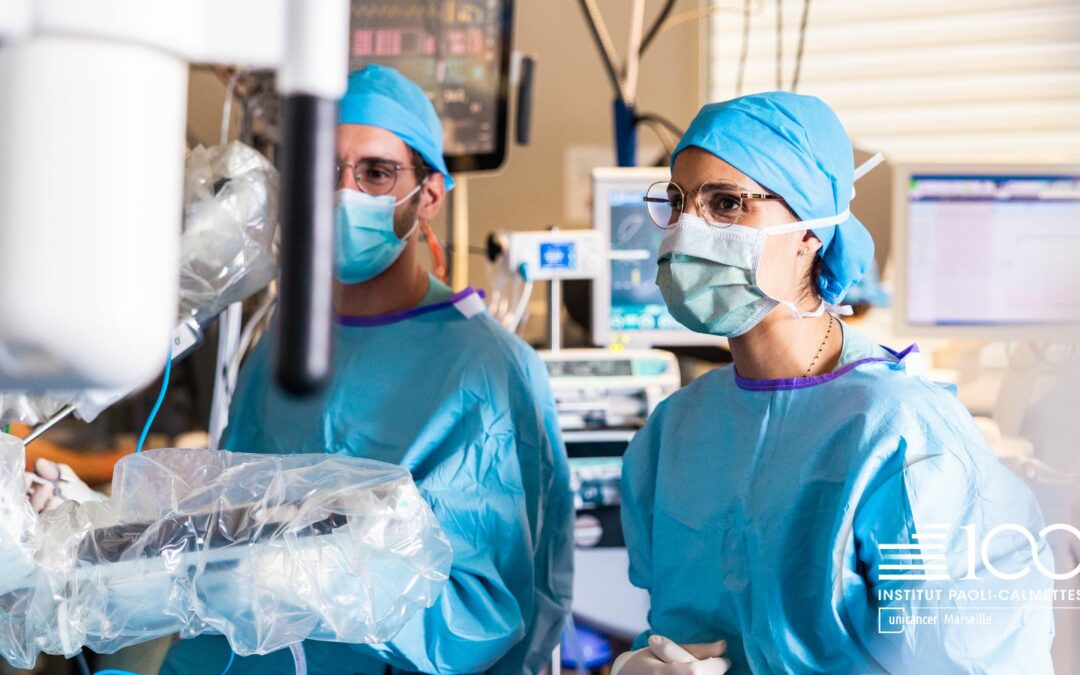
LA CHIRURGIE ONCOLOGIQUE HOLISTIQUE : RESULTAT DE 20 ANS D’INNOVATIONS A L’INSTITUT PAOLI-CALMETTES
Depuis 20 ans l’Institut Paoli-Calmettes (IPC) n’a eu de cesse de développer les innovations technologiques et organisationnelles en chirurgie oncologique, aboutissant aujourd’hui à une chirurgie oncologique que l’on pourrait qualifier d’holistique, destinée à tous les patients nécessitant un geste chirurgical pour la prise en charge d’un cancer.

Journée internationale de la recherche clinique
Ce 20 mai, à l’occasion de la Journée internationale de la recherche clinique, l’IPC met à l’honneur une de ses 3 missions principales : la recherche, et plus particulièrement la recherche clinique, au service de l’innovation et du progrès médical.

L’Institut Paoli-Calmettes remporte le prix « coup de cœur du public » aux Étoiles de l’Europe en Région Sud !
L’Institut Paoli-Calmettes remporte le Prix “Coup de cœur du public” des Étoiles de l’Europe en Région Sud pour son projet innovant « Big Data : l’EDS de l’IPC » !

Invitation Colloque sur le Don – 16 juin
Nous avons le plaisir de vous inviter au colloque « Le Don » qui se tiendra le 16 juin 2025 au Musée d’Histoire de Marseille.
Cet événement est gratuit et ouvert à tous !